Termodinamika Teknik Kimia: Heat Effect
January 30, 2018Materi Teknik Kimia, Termodinamika: Heat Effect
Referensi: Introduction to Chemical Engineering Thermodynamics 7th Ed (Smith, Van Ness, Abbott)
Heat Effect
Secara umum, banyak sekali proses kimia yang melibatkan perpindahan panas. Beberapa jenis transfer panas tersebut adalah panas/kalor sensibel, kalor laten, kalor reaksi, kalor pencampuran.
Sensible Heat
Kalor yang terlibat ketika tidak ada perubahan fasa, reaksi kimia, atau perubahan tekanan/volume yang menyebabkan terjadinya perubahan temperatur.
Persamaan diatas valid pada kondisi isobarik, gas ideal, low pressure gas, dan sistem tertutup.
Sementara itu, untuk kondisi isovolume, persamaan berikut yang berlaku:
Kapasitas Panas (Temperature Dependance)
Persamaan yang menghubungkan antara kapasitas panas dengan temperatur ditunjukkan dibawah ini
Dengan nilai A, B, C, dan D adalah konstanta-konstanta yang nilainya bergantung dari jenis senyawa atau komponen yang terlibat. Data tersebut telah ditabulasi dan lengkapnya bisa dilihat pada lampiran buku-buku terkait karangan Smith, Van Ness, Abbott, atau Daubert
Pada tabel tersebut, nilai A, B, C, D adalah untuk Cp/R, sehingga satuan dari Cp akan bergantung dari satuan R yang digunakan. Beberapa nilai R dengan satuan yang berbeda dapat dilihat di wikipedia pada link berikut
Untuk campuran gas dan cairan, kapasitas panas dapat pula dihitung dengan melibatkan fraksi/komposisinya :
Kapasitas Panas Rata-Rata(Temperature Dependance)
Untuk mempermudah perhitungan, perlu didefinisikan kapasitas panas rata-rata yang diturunkan dari persamaan sebelumnya hingga didapat persamaan berikut:
Sehingga perhitungan kalor untuk kasus isobarik dapat ditulis sebagai berikut
Perlu diperhatikan bahwa satuan T pada persamaan tersebut adalah dalam Kelvin.
Seluruh persamaan diatas dapat ditulis pula ditulis dalam variabel T1 dan T2:
Latent Heat
Kalor laten adalah kalor yang terlibat saat terjadinya perubahan fasa dan tidak ada perubahan temperatur. Kalor laten terlibat ketika misalnya suatu cairan berubah fasa menjadi padat, atau dari cair menjadi uap.
Perhitungan kalor laten dapat dilakukan menggunakan rumus Clapeyron diatas dengan menggunakan data Psat, Tsat, Vsat liq, dan Vsat vap. Cara lain yang dapat dilakukan namun khusus untuk air adalah pada steam table yang mana akan didapat nilai Hsat vap dan Hsat liq dan nilai kalor latennya adalah selisih antara keduanya.
Persamaan lain yang dapat digunakan adalah Persamaan Riedl dan Persamaan Watson.
Lebih lanjut, bisa kunjungi wikipedia pada link berikut
Kalor Reaksi
Dengan menggunakan data Kalor pembentukan pada temperatur 298 K, Kalor suatu reaksi dapat dihitung dengan menggunakan persamaan berikut:
dengan vi adalah koefisien suatu senyawa pada persamaan reaksi. Diberi tanda minus (-) bila senyawa tersebut berperan sebagai reaktan.
Untuk temperatur selain temperatur 298 K, nilai kalor reaksi pada temperatur T dapat dihitung sebagai berikut:
Huruf M tersebut dapat diganti dengan A, B, C, dan D.









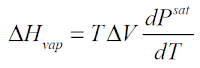


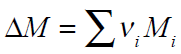



1 comments
This comment has been removed by the author.
ReplyDelete